安徽進(jìn)口生物試劑高鹽核酸酶70950-202
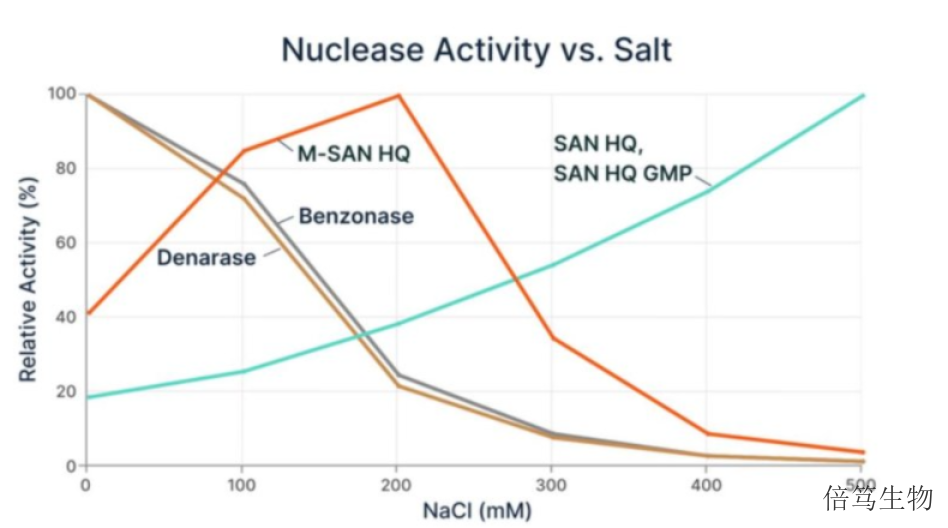
SANHQ(Bioprocessinggrade)是一種新型的、耐高鹽的工程化內(nèi)切酶。該酶在0.5MNaCl條件下具有良好活性,是大規(guī)模生產(chǎn)及生物工藝流程中去除核酸污染的理想選擇。鹽濃度是純化工藝的重要參數(shù)之一,高鹽濃度能夠減少聚集、增加目標(biāo)產(chǎn)物溶解度及提高目標(biāo)產(chǎn)物產(chǎn)量。高鹽濃度下,宿主DNA與蛋白質(zhì)能夠完全解離,從而更容易被降解。在藥物(如抗體、病毒載體藥物等)的生產(chǎn)及工藝流程中,核酸雜質(zhì)的去除至關(guān)重要。US FDA指南要求:zhiliao用重組生物制品終產(chǎn)品中,核酸雜質(zhì)含量低于100 pg/dose。SAN HQ獨特的耐高鹽特性、合規(guī)的生產(chǎn)體系標(biāo)準(zhǔn),讓其成為大規(guī)模生產(chǎn)工藝中核酸處理的理想選擇。常州高鹽核酸酶產(chǎn)品質(zhì)量哪家好呢,歡迎咨詢上海倍篤生物 。安徽進(jìn)口生物試劑高鹽核酸酶70950-202
從國內(nèi)來看,由于 AAV 基因藥物研發(fā)管線絕大部分集中在眼科遺傳病上,載體用量較小,三質(zhì)粒共轉(zhuǎn)染 AAV 系統(tǒng)足以滿足未來的臨床及商業(yè)需求,因此,國內(nèi)的 AAV 生產(chǎn)系統(tǒng)主要以三質(zhì)粒為主。然而,考慮到未來 AAV 基因藥物在血液、神經(jīng)系統(tǒng)、肌肉系統(tǒng)等領(lǐng)域的臨床應(yīng)用,三質(zhì)粒系統(tǒng)顯然難以勝任。如藥明生基從國外收購了 OXGENE 的輔助腺病毒 AAV 生產(chǎn)系統(tǒng) TESSA,據(jù)報道較三質(zhì)粒系統(tǒng)有10倍的提升;而基因藥物 CDMO 企業(yè)北京五加和基因則在國內(nèi)率先采用了陳海峰博士的威洛克公司授權(quán)的Bac-to-AAV 系統(tǒng),憑借公司在病毒載體領(lǐng)域持續(xù)30年的研發(fā)經(jīng)驗,不斷摸索、試驗,終于在臨床級生產(chǎn)方面獲得了巨大的成功,為 AAV 基因藥物管線研發(fā)公司錦籃基因進(jìn)行多批次臨床 CDMO 代工生產(chǎn)。海南基因藥物生產(chǎn)用高鹽核酸酶70921SAN HQ高鹽核酸酶的檢測標(biāo)準(zhǔn),都符合USP-EP要求。
經(jīng)典的慢病毒載體(LV)的生產(chǎn)工藝如下,——三質(zhì)粒系統(tǒng)瞬時轉(zhuǎn)染HEK293細(xì)胞系,轉(zhuǎn)染24小時后LV由轉(zhuǎn)染陽性細(xì)胞生產(chǎn)并排出到培養(yǎng)上清液中;收獲上清培養(yǎng)液后,加入核酸酶去除HCD污染,通過澄清步驟去除大的細(xì)胞碎片等雜質(zhì);下游純化步驟分離LV載體,純化方法包括切向流過濾TFF、色譜純化及超速離心;純化后的LV病毒顆粒經(jīng)過無菌過濾,更換到優(yōu)化后的配方中,灌裝并冷凍保存。每批Car-T生產(chǎn)時取對應(yīng)量的LV病毒,切忌反復(fù)凍融,否則LV病毒會失活。
ArcticZymes廠家對鹽活性核酸酶系列產(chǎn)品(Salt Active Nucleases,SANs)的生產(chǎn)及質(zhì)控,包括SAN HQ高鹽核酸酶和M-SAN HQ中鹽核酸酶,在符合ISO13485:2016體系基礎(chǔ)上,增加了cGMP質(zhì)控標(biāo)準(zhǔn),如microbes、endotoxin、蛋白酶等;同時提供TSE/BSE聲明、無動物源(Animal-Origin Free)聲明、非轉(zhuǎn)基因聲明等文件協(xié)助藥物申報。此外,ArcticZymes的生產(chǎn)場地接受客戶的定期審計,其第三方審計文件已得到國際TOP CDMO及Biotech的認(rèn)可,并已經(jīng)成為國際TOP CDMO的供應(yīng)商。具體文件體系可以跟廠家或?qū)?yīng)銷售人員聯(lián)系。蘇州高鹽核酸酶哪家好呢,歡迎咨詢上海倍篤生物 。
細(xì)胞基因藥物的基因遞送有病毒及非病毒兩種方式,其中病毒遞送更為常用。在病毒遞送路徑中,腺相關(guān)病毒(AAV)和慢病毒(Lentivirus)是常用的兩種載體;差別是病毒基因組的存在形式,AAV的基因組一般不整合到染色體中,以游離形式存在于染色體之外,且一般會表達(dá)數(shù)年之久;而慢病毒的基因組則會整合到染色體達(dá)到長期持續(xù)表達(dá)的目的。此外,其它用于基因藥物的病毒載體有單純皰疹病毒(HSV)、痘苗病毒(Vaccina Virus)、痘病毒(Poxviruses)。ArcticZymes Technologies旨在是研究和開發(fā)具有獨特特性的酶。海南基因藥物生產(chǎn)用高鹽核酸酶70921
徐州高鹽核酸酶售后服務(wù)哪家好呢,歡迎咨詢上海倍篤生物 。安徽進(jìn)口生物試劑高鹽核酸酶70950-202
監(jiān)管部門對HCD的殘留量有明確的規(guī)定。美國FDA發(fā)布的指導(dǎo)原則中指出生物制品HCD殘余限度為 100pg/劑,對于大劑量生物制品如單克隆抗體,根據(jù)其殘留DNA來源及給藥途徑,殘留量可放寬至 10ng/劑。細(xì)胞基因藥物終產(chǎn)品的DNA殘留有兩種來源,分別是宿主細(xì)胞DNA(HCD)和轉(zhuǎn)染用的質(zhì)粒。質(zhì)粒和HCD的存在形式不同,去除效率也差別很大。其中,質(zhì)粒是裸露的DNA雙鏈,帶強(qiáng)負(fù)電荷,通過色譜純化主要是離子交換能夠很高效去除;HCD則是以核小體緊密折疊形成的染色質(zhì)形式存在,幾乎不以裸DNA形式存在,所以很難去除。安徽進(jìn)口生物試劑高鹽核酸酶70950-202
- 吉林高鹽核酸酶 2025-04-04
- 安徽基因藥物生產(chǎn)用高鹽核酸酶 2025-04-04
- 海南SAN HQ高鹽核酸酶70921-160 2025-04-04
- 四川SAN HQ TF高鹽核酸酶70921 2025-04-04
- 湖南ArcticZymes中鹽核酸酶70950-202 2025-04-04
- 山西等滲條件中鹽核酸酶70950-150 2025-04-04
- SAN HQ高鹽核酸酶70921-160 2025-04-04
- 河南基因藥物生產(chǎn)用高鹽核酸酶70921-150 2025-04-04
- M-SAN中鹽核酸酶70950-150 2025-04-04
- 福建M-SAN HQ中鹽核酸酶 2025-04-04
- 2 2025-04-05
- 銀杏葉提取物現(xiàn)貨 2025-04-05
- 重慶天然來源AKG源頭廠家 2025-04-05
- 金山區(qū)附近教育軟件怎么樣 2025-04-05
- 江蘇環(huán)氧乙烷滅菌時間 2025-04-05
- 安徽1200℃馬弗爐定制價格 2025-04-05
- 山西紫杉醇側(cè)鏈中間體(3R 2025-04-05
- 麗水矯形器假肢公司 2025-04-05
- 世格球囊穿刺器咨詢 2025-04-05
- 福建調(diào)拌碗口腔耗材價格 2025-04-05