富陽區免疫共培養基質膠-類器官培養實驗步驟
為克服基質膠的高成本和復雜性,懸浮培養(如低附著板)或合成支架(如聚乳酸納米纖維)逐漸興起。例如,肺*類***在磁性納米顆粒懸浮系統中能形成均一球體,且便于藥物篩選。生物打印技術也可直接堆疊細胞-生物墨水(如GelMA)構建類***陣列,提升通量。但無膠培養可能丟失關鍵ECM信號,導致極性或功能缺陷(如腎類***缺乏管腔結構),需通過添加ECM蛋白片段補償。基質膠類***已用于疾病建模(如囊性纖維化)、個性化藥敏測試(如結直腸*PDO)和再生醫學(如肝類***移植)。但挑戰包括:①批次間差異影響數據可比性;②免疫類***等復雜模型仍需優化膠成分;③規模化生產時膠的成本和操作難度。未來趨勢是開發標準化合成膠、結合器官芯片實現血管化,以及利用機器學習預測比較好培養條件。基質膠包裹類器官可防止細胞凋亡并維持結構完整性。富陽區免疫共培養基質膠-類器官培養實驗步驟
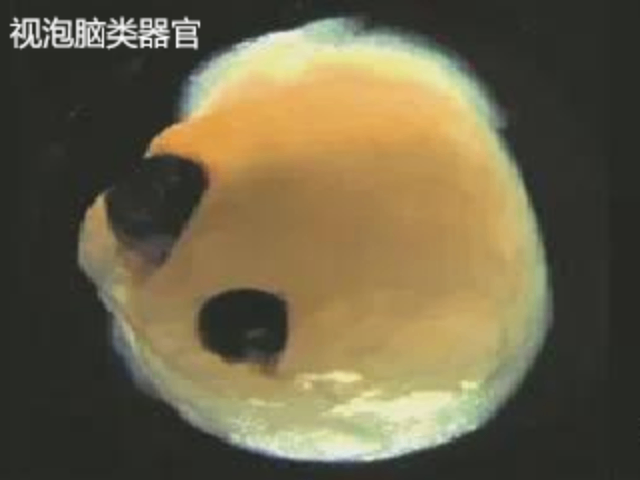
基質膠優化的類***模型在疾病研究中發揮重要作用。在**研究領域,患者來源類***(PDO)培養中基質膠的成分和硬度可模擬特定**微環境。囊性纖維化研究中,通過調整基質膠的離子組成可重現病理條件下的黏液分泌表型。神經退行性疾病模型中,基質膠的拓撲結構可影響β-淀粉樣蛋白的聚集行為。***進展是將基質膠培養的類***與微流控芯片結合,構建具有血管網絡的復雜疾病模型,為藥物篩選提供更真實的測試平臺。當前基質膠-類***技術面臨多個挑戰:①標準化問題,不同批次的天然基質膠存在差異;②復雜類***(如免疫類***)的培養方案仍需優化;③規模化生產的成本控制。未來發展方向包括:①開發化學成分明確的標準合成基質膠;②結合3D生物打印技術實現類***的精細構建;③整合多組學分析技術建立基質膠-類器官培養的預測模型。隨著材料科學和生物技術的進步,基質膠類***技術將在精細醫療和再生醫學領域發揮更大作用。臨安區腸道基質膠-類器官培養誰家好基質膠的流變學特性應匹配類器官培養的機械動態需求。
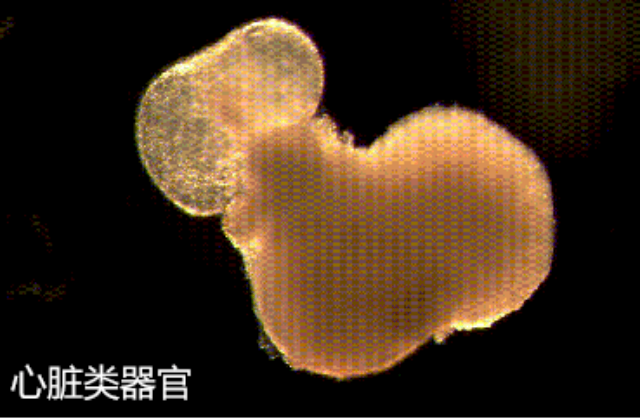
盡管基質膠類***技術取得***進展,仍面臨若干關鍵挑戰。標準化問題是首要障礙,不同批次的天然基質膠存在***差異,影響實驗可重復性。復雜類***模型的構建仍需突破,如具有完整免疫微環境的類***培養仍然困難。規模化生產面臨成本和技術雙重挑戰,特別是臨床級類***的培養要求。未來發展方向包括:開發化學成分明確的標準基質膠替代品;結合3D生物打印技術實現類***的精細構建;發展智能響應性材料模擬動態微環境變化;建立自動化培養和質量控制體系。隨著材料科學、干細胞技術和生物工程的交叉融合,基質膠類***技術有望在疾病建模、藥物開發和再生醫學等領域發揮更大作用。特別值得關注的是器官芯片技術的發展,將為基質膠類***提供更接近體內的培養環境。
基質膠(Matrigel)是一種由基底膜成分組成的生物材料,主要來源于小鼠的腫瘤細胞,富含膠原蛋白、層粘連蛋白、糖胺聚糖等多種生物活性分子。其獨特的三維結構為細胞提供了一個接近自然環境的培養基,使細胞能夠在更接近體內的條件下生長和分化。基質膠的物理和化學特性使其成為類培養的理想選擇。由于其良好的生物相容性和生物降解性,基質膠能夠支持細胞的粘附、增殖和分化,促進細胞間的相互作用,從而更好地模擬體內微環境。此外,基質膠的凝膠化特性使其能夠在體外形成三維結構,為類的形成提供了必要的支撐。基質膠為類器官提供仿生微環境,促進三維結構形成。
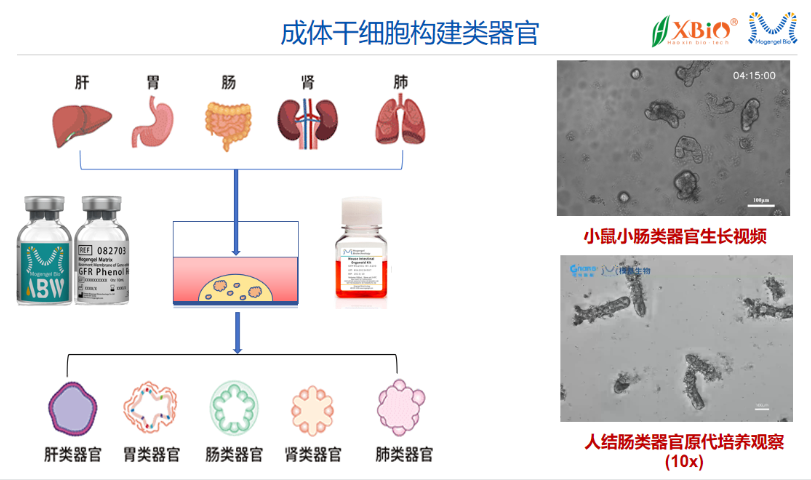
基質膠(Extracellular Matrix, ECM)是一種復雜的生物材料,主要由多種蛋白質和多糖組成,***存在于動物和植物的細胞外環境中。它不僅為細胞提供結構支持,還在細胞的生長、分化和遷移等生物過程中發揮重要作用。在類***培養中,基質膠作為細胞生長的支架,能夠模擬體內微環境,為細胞提供必要的生物信號和物理支持。基質膠的組成和物理特性可以根據不同的細胞類型和實驗需求進行調節,從而優化類***的培養條件。通過調控基質膠的硬度、孔隙率和生物活性,研究人員能夠更好地控制細胞的行為,促進類***的形成和成熟。基質膠的彈性模量調控類器官的干性維持或分化傾向。嘉興基質膠-類器官培養價位
優化基質膠濃度可顯著提高類器官存活率和增殖效率。富陽區免疫共培養基質膠-類器官培養實驗步驟
盡管基質膠在類***培養中具有諸多優勢,但仍然面臨一些挑戰。例如,類***的異質性和可重復性問題可能影響實驗結果的可靠性。此外,類***的培養周期較長,且對培養條件的要求較高,增加了實驗的復雜性。為了解決這些問題,研究人員正在探索新的培養基和支撐材料,以提高類***的形成效率和穩定性。例如,使用合成聚合物或其他天然基質作為替代材料,可能會改善類***的生長環境。此外,采用高通量篩選技術,可以加速對不同培養條件的優化,從而提高類***的可重復性和實驗效率。富陽區免疫共培養基質膠-類器官培養實驗步驟
- 蘭溪單核細胞趨化蛋白3(MCP3)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 揚州促卵泡素(FSH)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 義烏補體因子D(CFD)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 太倉血紅蛋白(HB)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 昆山血管生長素(ANG)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 龍港基質金屬蛋白酶8(MMP8)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 溧陽白介素1受體拮抗劑(IL1RA)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 衢州鐵蛋白(FE)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 上海表面活性物質關聯蛋白D(SPD)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 鹽城卵白蛋白(OVA)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 外泌體提取和檢測品牌 2025-04-26
- 南京滅菌凍存管客服電話 2025-04-26
- 江西特殊氣氛箱式爐類型 2025-04-26
- 長沙抗蛋白涂層 2025-04-26
- 普通實驗室細胞灌裝設備維保時間 2025-04-26
- 廣東草本足浴粉去哪買 2025-04-26
- 上海比較好的分子耗材 2025-04-26
- 蘭溪單核細胞趨化蛋白3(MCP3)檢測試劑盒(酶聯免疫吸附試驗法) 2025-04-26
- 同濟生物紅參粉批發 2025-04-26
- 甘肅食用益生菌作用 2025-04-26