長沙外泌體提取試劑
所有培養(yǎng)的細(xì)胞類型均可分泌外泌體,且外泌體天然存在于體液中,包括血液、唾液、尿液、腦脊液和乳汁中。有關(guān)他們分泌和攝取及其組成、“運(yùn)載物”和相應(yīng)功能的精確分子機(jī)制剛剛開始研究。外泌體目前被視為特異性分泌的膜泡,參與細(xì)胞間通訊,對外泌體的研究興趣日益增長,無論是研究其功能還是了解如何將其用于微創(chuàng)診斷的開發(fā)。1983年,外泌體初次于綿羊網(wǎng)織紅細(xì)胞中被發(fā)現(xiàn),1987年Johnstone將其命名為“exosome”。多種細(xì)胞在正常及病理狀態(tài)下均可分泌外泌體。其主要來源于細(xì)胞內(nèi)溶酶體微粒內(nèi)陷形成的多囊泡體,經(jīng)多囊泡體外膜與細(xì)胞膜融合后釋放到胞外基質(zhì)中。外泌體的提取、分離方法:超高速離心法。長沙外泌體提取試劑

CD47是信號調(diào)節(jié)蛋白α(SIRPα,也稱為CD172a)的配體,CD47-SIRPα間的結(jié)合能夠發(fā)出“不要吃我”的信號,從而壓制吞噬作用。病基因RAS能夠促進(jìn)胰腺病細(xì)胞增殖,增強(qiáng)胞飲作用從而促進(jìn)一些病癥細(xì)胞攝取外泌體。合成納米顆粒對細(xì)胞有一定毒性作用,但使用外泌體能夠較小化對細(xì)胞的毒性。研究人員發(fā)現(xiàn),CD47和病基因KRAS驅(qū)動的胞飲作用都會壓制外泌體被循環(huán)系統(tǒng)的清理,并增強(qiáng)胰腺病細(xì)胞對外泌體的特異性。所以,外泌體的這種特性增強(qiáng)了它們通過遞送RNAi來特異性靶向胰腺病中的KRAS的能力,并且使用外泌體作為單一靶向劑顯著改善了所有實(shí)驗(yàn)PDAC小鼠模型的總生存期。蕪湖正規(guī)外泌體提取試劑廠家來源于細(xì)胞內(nèi)溶酶體微粒內(nèi)陷形成的多囊泡體,經(jīng)多囊泡體外膜與細(xì)胞膜融合后釋放到胞外基質(zhì)中。
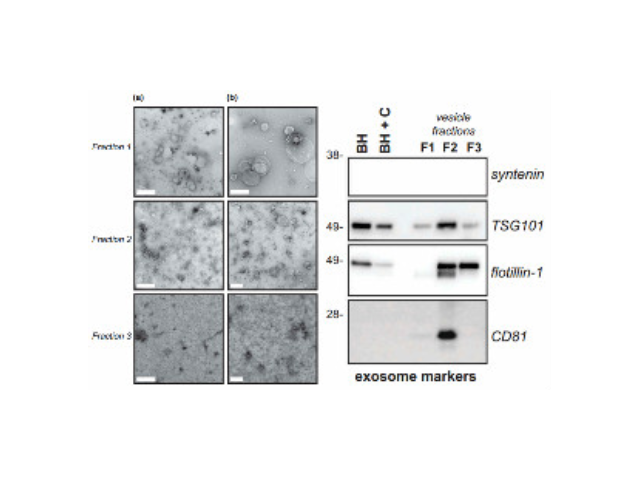
外泌體項(xiàng)目獲批學(xué)科方向:從統(tǒng)計來看,與前年相似外泌體立項(xiàng)集中的領(lǐng)域還是一些病癥學(xué),近年來外泌體發(fā)表的文章也絕大部分與其在一些病癥的形成,耐藥性,檢測等方面有關(guān)。例如2019年發(fā)表在MolecularCancer(IF=10.679)上的文章表明外泌體FMR1-AS1通過TLR7/NFκB/c-My信號通路在女性食管ai中促進(jìn)維持ai癥干細(xì)胞樣細(xì)胞的動態(tài)平衡。發(fā)表在JournalofExperimental&ClinicalCancerResearch(IF=5.646)上的一篇文章發(fā)現(xiàn)外泌體轉(zhuǎn)運(yùn)p-STAT3可促進(jìn)結(jié)直腸ai細(xì)胞獲得性5-FU耐藥性。發(fā)表在Cancers(IF=6.162)上的一篇文章則研究了腹腔灌洗液中細(xì)胞外囊泡相關(guān)的miRNA作為子宮內(nèi)膜ai分子標(biāo)志物的可能性。此外,在神經(jīng)系統(tǒng)和精神疾病,中醫(yī)學(xué)及其他領(lǐng)域也有不少外泌體相關(guān)項(xiàng)目中標(biāo)。外泌體提取試劑直銷價外泌體檢測作為一種新型的液體活檢熱點(diǎn)技術(shù)已被許多臨床科研機(jī)構(gòu)普遍地應(yīng)用于一些病癥和疾病的無創(chuàng)診斷
外泌體的提取、分離方法:開發(fā)高效、快速、穩(wěn)定,并且保持外泌體結(jié)構(gòu)和生物功能完整性的方法,是目前外泌體應(yīng)用于臨床的基礎(chǔ)和前提。從細(xì)胞上清和體液中提取分離外泌體的方法很多,但是外泌體的純度和產(chǎn)量卻和分離方法息息相關(guān)。通常分離步驟少、產(chǎn)率高,但是純度會受到影響。鑒于每種分離方法都有其優(yōu)缺點(diǎn),實(shí)驗(yàn)可以根據(jù)樣本來源、下游實(shí)驗(yàn)?zāi)康牡龋x擇合適的外泌體分離方法。2015年,國際囊泡組織(InternationSocietyforExtracelluarVesicles,ISEV)指出,簡單依靠一種分離方法得到的外泌體的純度和產(chǎn)量都難滿足實(shí)驗(yàn)的需求。因此,推薦聯(lián)合使用各種方法,從而得到高純度和高產(chǎn)量的外泌體。目前人們多采用超速離心、免疫磁珠、超濾、沉淀或試劑盒等方法實(shí)現(xiàn)外泌體的提取分離。

外泌體研究的主要應(yīng)用:外泌體的功能取決于其所來源的細(xì)胞類型,其可參與到機(jī)體免疫應(yīng)答、抗原提呈、細(xì)胞遷移、細(xì)胞分化、一些病癥侵襲等方方面面。有研究表明一些病癥來源的外泌體參與到一些病癥細(xì)胞與基底細(xì)胞的遺傳信息的交換,從而導(dǎo)致大量新生血管的生成,促進(jìn)了一些病癥的生長與侵襲。一些病癥。一些病癥轉(zhuǎn)移。來自白血病干細(xì)胞的外泌體促進(jìn)急性骨髓性白血病(AML)細(xì)胞的增殖、遷移和壓制細(xì)胞凋亡。治病靶標(biāo)。利用外泌體遞送小干擾RNA來沉默KRASG12D,從而特異性高效靶向至胰腺病細(xì)胞,以明顯降低RAS活化、病細(xì)胞增殖和轉(zhuǎn)移過程。免疫。β細(xì)胞將含有蛋白質(zhì)和miRNA的外泌體釋放到細(xì)胞外,并可轉(zhuǎn)移到其他代謝部位或免疫內(nèi)皮細(xì)胞,有利于維持葡萄糖體內(nèi)平衡或造成胰島素抵抗。心血管。外泌體介導(dǎo)miR-155從平滑肌細(xì)胞轉(zhuǎn)移到內(nèi)皮細(xì)胞導(dǎo)致了內(nèi)皮細(xì)胞的損傷促進(jìn)動脈硬化。分子標(biāo)記。疾病診斷。在酒精性肝病、NASH、菌類性肝炎、藥物性肝損傷和肝細(xì)胞病中發(fā)現(xiàn)循環(huán)EVs的水平上升。預(yù)后標(biāo)志。外泌體提純試劑盒的特色與優(yōu)勢:純化和富集的完整血漿/血清,尿液和細(xì)胞培養(yǎng)基中外泌體可用于功能研究。珠海外泌體提取試劑生產(chǎn)廠家
外泌體提取:超離法因操作簡單,獲得的囊泡數(shù)量較多而廣受歡迎。長沙外泌體提取試劑
外泌體(Exosome)是細(xì)胞主動分泌的囊泡樣小體,大小均一,直徑30-200nm,密度1.10-1.18g/ml,來源普遍,幾乎所有細(xì)胞都可分泌,在血液,尿液,唾液,腦脊液,腹水,乳汁等體液中普遍分布。外泌體較早在1986年發(fā)現(xiàn)于培養(yǎng)的綿羊紅細(xì)胞上清液中。1996年,研究者發(fā)現(xiàn)外泌體作為抗原呈遞因子參與T細(xì)胞依賴的抗一些病癥反應(yīng),開啟了外泌體蛋白研究的新天地。2013年諾貝爾生物/醫(yī)學(xué)獎解答了細(xì)胞如何組織其內(nèi)部較重要的運(yùn)輸系統(tǒng)之一——囊泡傳輸系統(tǒng)的奧秘。超離法因操作簡單,獲得的囊泡數(shù)量較多而廣受?歡迎,但過程比較費(fèi)時,且回收率不穩(wěn)定,純度也受到質(zhì)疑。長沙外泌體提取試劑
- 溫州正規(guī)無血清細(xì)胞凍存液單價 2025-05-03
- 開封正規(guī)RNA提取試劑銷售廠家 2025-05-03
- 成都無血清細(xì)胞凍存液銷售廠家 2025-05-03
- 南昌正規(guī)RNA提取試劑廠家現(xiàn)貨 2025-05-03
- 溫州濟(jì)南無血清細(xì)胞凍存液 2025-05-03
- 南昌無血清細(xì)胞凍存液廠家直銷 2025-05-03
- 珠海正規(guī)RNA提取試劑推薦廠家 2025-05-03
- 鄭州RNA提取試劑報價 2025-05-03
- 貴陽外泌體提取試劑單價 2025-05-03
- 杭州正規(guī)無血清細(xì)胞凍存液廠家現(xiàn)貨 2025-05-03
- 酸催化劑哪家好 2025-05-03
- 溫州正規(guī)無血清細(xì)胞凍存液單價 2025-05-03
- 天津陰離子丁苯膠乳價格 2025-05-03
- 常州半合成切削液廠家 2025-05-03
- 開封正規(guī)RNA提取試劑銷售廠家 2025-05-03
- 江西客制化水處理設(shè)備批發(fā) 2025-05-03
- 成都無血清細(xì)胞凍存液銷售廠家 2025-05-03
- 山東環(huán)保型聚氨酯膠陶瓷修復(fù) 2025-05-03
- 陜西3N碲錠廢料回收 2025-05-03
- 南昌正規(guī)RNA提取試劑廠家現(xiàn)貨 2025-05-03