北京哺乳動物紡錘體兼容大部分顯微鏡
減數分裂是生物體形成配子(精子和卵子)的過程,其特點是一次DNA復制后細胞連續分裂兩次,形成四個遺傳物質相似的子細胞。在減數分裂過程中,紡錘體同樣發揮著至關重要的作用。在減數分裂Ⅰ的前期,同源染色體發生配對、聯會、交換和交叉,形成四分體。這一過程依賴于紡錘體的微管網絡,它確保了同源染色體能夠正確地配對和交換遺傳信息。隨后,在減數分裂Ⅰ的中期,染色體在紡錘絲的牽引下,排列在赤道板上。與有絲分裂不同的是,此時排列在赤道板上的染色體是同源染色體對,而不是姐妹染色單體。當細胞進入減數分裂Ⅰ的后期,同源染色體在紡錘體的牽引下分離,分別移向細胞的兩極。這一過程實現了同源染色體的分離,為后續的遺傳重組和配子形成奠定了基礎。在減數分裂Ⅱ中,紡錘體的作用與有絲分裂更為相似。姐妹染色單體在紡錘絲的牽引下分離,分別移向細胞的兩極。這一過程確保了每個子細胞都能獲得完整的染色體組,從而保證了配子的遺傳完整性。 紡錘體在細胞分裂中的功能受到嚴格的時間和空間控制。北京哺乳動物紡錘體兼容大部分顯微鏡
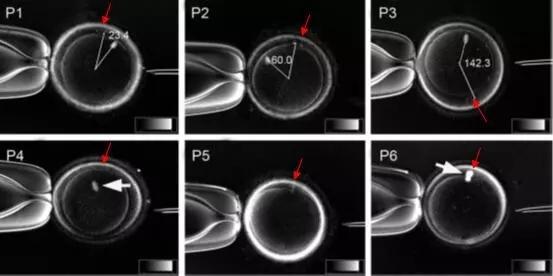
秋水仙素為什么會使有絲分裂的細胞停滯于中期如果用秋水仙素處理有絲分裂的細胞,紡錘體會迅速消失,細胞停滯在有絲分裂中期,染色體無法分離成兩組。用秋水仙堿進行誘導,從而將細胞阻斷在細胞分裂中期,也是誘導細胞周期同步化的重要方法之一。真核細胞周期可分為4個時期,分別是G1期、S期、G2期和M期。在細胞周期調控中主要有3個控制點,***個控制點在G1期,決定細胞能否進入S期;第二個控制點在G2期,決定細胞能否進入有絲分裂期;第三個控制點在M期,決定細胞是否已經準備好將復制好的染色體拉向兩極。CDK(周期蛋白依賴性蛋白激酶)對細胞周期運行起著**性調控作用,CDK與不同時期的周期蛋白結合會在特定周期起調節作用。cyclinA、cyclinB是在M期起調節功能的兩種主要周期蛋白。細胞周期運轉到分裂中期后,在后期促進復合物(APC)的作用下,M期cyclinA和cyclinB通過泛素化途徑迅速降解,Cdkl活性喪失,細胞周期便從M期中期向后期轉化。APC活性變化是細胞周期由分裂中期向后期轉換的關鍵因素,其活性受到多種因素的綜合調節,紡錘體組裝檢查點是其重要的調控因素。紡錘體組裝不完全,或所有動粒不能被動粒微管全部捕捉,則APC不能被***。昆明Hamilton Thorne紡錘體Oosight Basic紡錘體的形成與細胞骨架的重構密切相關。
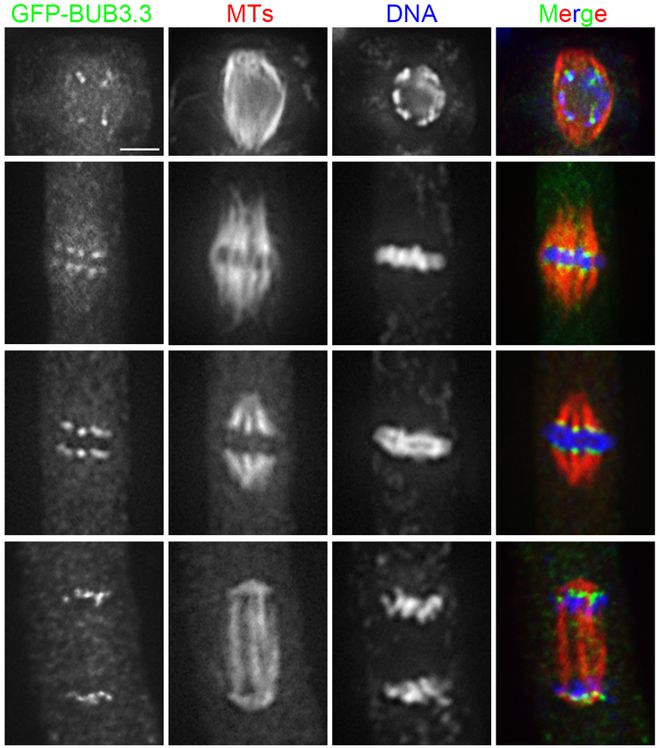
紡錘體的雙極化是卵母細胞減數分裂過程中的關鍵事件之一。近年來,我國學者在人類卵母細胞紡錘體雙極化機制研究方面取得了重要進展。通過高分辨成像技術,研究者們揭示了人類卵母細胞紡錘體雙極化的獨特機制,并發現了調控此過程的關鍵蛋白。這些研究成果不僅為雙折射性紡錘體卵冷凍研究提供了新的視角和思路,也為臨床生殖障礙疾病的診療提供了科學依據。隨著偏光成像技術和冷凍保護劑研究的不斷深入,未來有望開發出更加高效、安全的卵母細胞冷凍保存方案。例如,通過改進冷凍速率和程序、優化保護劑配方等手段,進一步減輕冷凍損傷,提高解凍后卵母細胞的存活率和發育潛能。
阿爾茨海默病患者中,微管蛋白(如tau蛋白)的突變和異常磷酸化會影響微管的穩定性和紡錘體的組裝,導致染色體分離異常和細胞周期紊亂。紡錘體功能障礙會導致染色體不穩定,增加基因組的不穩定性,進而影響神經元的正常功能和存活。正常情況下,成熟的神經元處于G0期,不會重新進入細胞周期。然而,阿爾茨海默病患者中,神經元可能會重新進入細胞周期,但由于紡錘體功能障礙,無法完成正常的細胞分裂,導致細胞凋亡。在神經元中,紡錘體的正常功能對于神經元的發育、分化和維持至關重要。 紡錘體在細胞分裂后期推動染色體向細胞兩極移動。
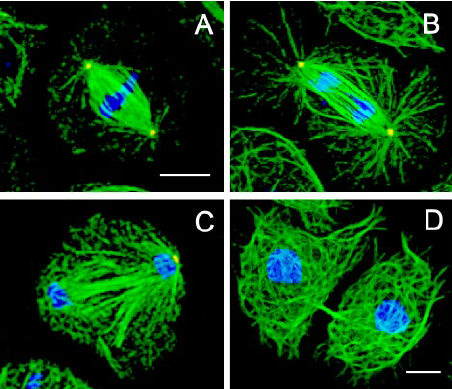
胞質膜在動物細胞的細胞分裂結束時,母細胞在一個被稱為“胞質分裂”的過程中分裂成兩個子細胞和分區隔離的染色體。有絲分裂紡錘體控制胞質膜上的“胞質分裂”事件,但連接這兩個宏觀結構的機制一直不清楚。MarkPetronczki及其同事提供了一個結構和功能分析結果,他們發現**紡錘體蛋白(紡錘體中間區域和中間體中的一個蛋白復合物)是有絲分裂紡錘體與胞質膜間所缺失的聯系環節,這個聯系環節確保“胞質分裂”過程的***結果。本文作者還發現,**紡錘體蛋白的MgcRac***亞單元中的一個區域為一個“系繩”,它連接到胞質膜中的磷酸肌醇脂質上。[4]紡錘體的一端連接著染色體,另一端則錨定在細胞兩極。昆明ICSI紡錘體透明帶
紡錘體微管的動態變化是細胞分裂周期的重要標志。北京哺乳動物紡錘體兼容大部分顯微鏡
紡錘體生成在含中心體的細胞中,紡錘體的生成開始于細胞分裂前初期-即在細胞核膜分解(NuclearEnvelopeBreakdown,NEB)之前。初期的結構為兩個**的以中心體為核的星狀體(asters)。當細胞核膜分解后,染色體和星狀體發生一系列復雜的互動反應。**終結果為所有的染色體在紡錘體的**(赤道板,)排列整齊,每兩條染色體有一個著絲點,每一個著絲點被一束極性相同的微管(通常稱為紡錘絲)附著。此時細胞處于分裂中期,紡錘體生成完畢。實驗證明,中心體在這個過程中的作用不是必需的。動物細胞在中心體被激光搗毀后仍舊能夠筑構紡錘體,但其位置通常不在細胞的大致幾何中心,其后的胞質分裂也會受嚴重影響。紡錘體[1]在不含中心體的細胞中,紡錘體的生成是由染色體本身主導的。此過程由一小分子量的GTP連接蛋白(RanGTPase)控制。細胞核分解后,紡錘絲由染色體周圍生成。其后這些紡錘絲會在動力分子與為微管動力的合作影響下自動排列為極性相反大致數目相同的兩組。每組的極性相對于一組著絲點。同時在微管遠端的動力蛋白dynein會將這些微管束集中到一點,形成紡錘極區(SpindlePolarZone)。與此同時,染色體會自動在赤道板排列整齊。紡錘體生成完畢。北京哺乳動物紡錘體兼容大部分顯微鏡
- 北京哺乳動物紡錘體胚胎植入 2025-04-07
- 深圳克隆紡錘體兼容大部分顯微鏡 2025-04-07
- 美國MII期紡錘體液晶偏光補償器 2025-04-07
- 香港非侵入式成像紡錘體Oosight Basic 2025-04-07
- 美國核移植紡錘體卵質量評估 2025-04-07
- 昆明非侵入式成像紡錘體卵細胞評價 2025-04-07
- 昆明雙折射性紡錘體價格 2025-04-07
- 昆明ICSI紡錘體卵細胞評價 2025-04-07
- 北京輔助生殖紡錘體Hoechst染料 2025-04-07
- 北京哺乳動物紡錘體兼容大部分顯微鏡 2025-04-07
- 重慶加工蛋品質分析儀 2025-04-07
- 蘭州光電式編碼器哪個品牌好 2025-04-07
- 山西穩定性甲醛試驗箱采購 2025-04-07
- 合肥旋轉博勒飛錐板粘度計 2025-04-07
- 廣東移液管實驗室用品供應商 2025-04-07
- 汕尾液貨艙監測報警系統哪家好 2025-04-07
- 遼寧在線濁度分析儀表廠家 2025-04-07
- 福建智能化單點式傳感器內容 2025-04-07
- 西藏彈簧微啟式外螺紋安全閥原理 2025-04-07
- 寧夏門尼粘度儀DMV2025哪家靠譜 2025-04-07